Organisme planctonique, microscopique
Lorica caractéristique en forme de cloche
Codonella campanella Haeckel, 1873
Codonella campanula Fol, 1884
Tintinnus campanula Ehrenberg, 1840
Synonyme probable : Tintinnopsis bütschlii Daday, 1887
Atlantique Nord-Est; espèce probablement cosmopolite
Zones DORIS : ● Europe (côtes françaises), ○ [Atlantique Nord-Est, Manche et mer du Nord françaises], ● Atlantique Nord-OuestTintinnopsis campanula est observé dans l’Atlantique Nord-Est, depuis les côtes africaines jusqu’à la Norvège, ainsi qu'en mer de Barents, en mer du Nord, en mer Baltique, en mer Méditerranée (notamment en Adriatique), en mer Noire et en mer Rouge.
Sa répartitions'étend également à l’Atlantique Nord-Ouest, où l'espèce est signalée dans les eaux de Nouvelle-Ecosse.
Elle est aussi mentionnée sur les côtes de l'Inde, de la Corée et du Japon.
Tintinnopsis campanula est une espèce planctonique*, vivant principalement dans les eaux superficielles, le plus souvent en zone côtière et jusque dans les estuaires.
Sa large plage de répartition traduit une grande tolérance thermique (espèce eurytherme*) ainsi qu’une large tolérance aux variations de salinité (espèce euryhaline*).
L’espèce se rencontre majoritairement dans les premiers mètres de la colonne d’eau, à proximité de la surface.
Tintinnopsis campanula est un tintinnide. Les tintinnides sont des protozoaires ciliés microscopiques
produisant une tunique protéique appelée lorica* (terme issu de la cuirasse portée par les légionnaires
romains). L’organisme vivant, dont les cils émergent de la lorica lors
de l’alimentation ou du déplacement, est observé plus rarement que la lorica
vide.
Le cilié*, lorsqu’il est rétracté, occupe environ la moitié du volume offert par la lorica.
La lorica de Tintinnopsis campanula présente une forme en cloche facilement reconnaissable. L’extrémité orale est évasée, la section centrale est cylindrique et l’extrémité aborale* présente une «queue» plus ou moins droite. Cette « queue » peut être absente chez certaines formes morphologiques, notamment la forme bütschlii.
La surface de la lorica est généralement parsemée de particules solides (grains de quartz, spicules* d’éponge, morceaux de frustule de diatomée*, etc.) réparties de manière inégale. La densité de ces particules varie fortement selon les
individus : certaines loricas n’en présentent que quelques-unes tandis que
d’autres en sont presque entièrement recouvertes.
La lorica mesure généralement entre 100 et 200 µm de
longueur ; le diamètre de l’ouverture varie de 60 à 150 µm.
Il existe plusieurs espèces de Tintinnopsis, dont la lorica* est plus ou moins recouverte de grains solides
Tintinnopsis campanula est cependant la seule espèce
présente dans nos eaux à posséder cette lorica typiquement évasée en forme de
cloche.
Comme tous les tintinnides, Tintinnopsis campanula se nourrit principalement de nanoplancton* (2 µm à 20 µm). Le diamètre des proies capturées est corrélé au diamètre de l’ouverture orale de la lorica (il s’agit du diamètre avant l’évasement) : la taille maximale des proies ingérées est de 45 % de ce diamètre et la taille de capture préférée est de 25 % de ce diamètre. Une couronne ciliée entourant la bouche génère des courants
d’eau dirigeant les proies vers l’orifice oral.
Les tintinnides se reproduisent pas scissiparité*. L’un des deux protozoaires* reste dans la lorica* initiale tandis que l’autre, issu de la scission est éjecté. Initialement dépourvu de lorica, l’individu issu de la
division doit en construire une nouvelle
Le brassage génétique est assuré par la conjugaison de deux individus, au sein d’une lorica (ce qui suppose qu’un des deux individus abandonne sa lorica). Cette conjugaison isogame* peut être considérée comme une reproduction sexuée.
Un autre comportement de reproduction par conjugaison isogame* (fusion de gamètes* identiques) a été observé chez certaines espèces. Les conjugants demeurent reliés pendant plusieurs heures au
niveau de l’ouverture de la lorica.
Chez Tintinnopsis beroidea, un mode de reproduction anisogame* a également été décrit, impliquant des microgamètes* libres fusionnant avec des macrogamètes*.
Des péridiniens parasites* sont fréquemment rencontrés chez les Tintinnides, dont Tintinnopsis campanula (par exemple Duboscquella tintinnicola). Un même individu peut héberger simultanément plusieurs parasites à différents stades de développement.
Compte tenu de la difficulté à observer les caractéristiques du cilié vivant, la classification des tintinnides a très longtemps été fondée sur la forme de la lorica*. Or, plusieurs études, dont les travaux déjà anciens de Jan Hofker concernant spécifiquement Tintinnopsis campanula, ont montré que la forme de la lorica est particulièrement plastique (un tintinnide qui perd ou quitte sa lorica peut en reconstituer une de forme différente) et dépend notamment des conditions environnementales.
La classification actuelle des tintinnides repose encore largement sur des critères morphologiques et demeure probablement partiellement inadéquate. Les approches modernes, notamment fondées sur l’analyse moléculaire, devraient permettre d’améliorer significativement la compréhension phylogénétique de ce groupe.. On sait d’ores et déjà que le genre Tintinnopsis est paraphylétique* et qu’il n’appartiendrait pas du tout à la famille des Codonellidés à laquelle il est actuellement rattaché (voir les travaux de Charles Bachy & al., 2012).
Les tintinnides possèdent plusieurs noyaux, en nombre variable selon les espèces. On distingue des macronoyaux et des micronoyaux.
Les grains collés sur la surface de la lorica accroissent la trainée du protozoaire, et ralentissent donc sa descente dans la colonne d’eau. La lorica pourrait servir de protection contre les prédateurs. Elle pourrait également avoir un rôle dans la maîtrise de la flottabilité par le protozoaire. Les travaux de Per Jonsson (1989) ont montré que, chez Tintinnopsis campanula, la densité de la lorica conduit à orienter l’ouverture vers le haut, ce qui conduit le cilié à nager naturellement vers la surface (le sens de nage correspond à une traction par la couronne ciliée).
Le cilié est attaché à la lorica par un pédoncule* rétractile, qui lui permet de se rétracter très rapidement. Le protozoaire ne se déplace pas lorsqu’il est ainsi rétracté. La sortie de la lorica se déroule à une vitesse croissante et le protozoaire se met en mouvement peu avant la sortie complète de la couronne ciliée. En temps normal, les tintinnides se déplacent en permanence. Leur déplacement est particulièrement rapide et difficile à suivre en observation microscopique;
Les tintinnides peuvent abandonner leur lorica et continuent alors à nager «nus», avant de reconstituer une lorica.
Au-delà de la couronne ciliée bien visible, les tintinnides disposent d’une ciliature importante le long du corps, jouant notamment un rôle dans la construction de la lorica.
Les tintinnides constituent de potentiels bioindicateurs* des conditions environnementales. Khalied El-Damhougy & al. (2017) ont ainsi démontré que Tintinnopsis campanula peut être utilisé pour mesurer l’oxygène dissous, la salinité, le pH, les nitrates et les nitrites.
Les tintinnides jouent un rôle écologique majeur car ils sont un maillon clef dans les chaînes trophiques* entre le nanoplancton et les planctonophages* de taille plus importante (copépodes* et larves* de crustacés notamment). Ils peuvent par ailleurs exercer une pression significative sur le phytoplancton*, notamment lors des blooms* phytoplanctoniques. Les populations de Tintinnopsis campanula peuvent alors
connaître des proliférations importantes.
Tintinnopsis campanula est l’un des tintinnides les plus fréquents dans les prélèvements de plancton* côtier réalisés en Manche et en mer du Nord.
Tintinnide campanule : appellation reprenant le nom du
groupe des tintinnides associée à la francisation du terme spécifique
campanula.
Tintinnopsis: ce nom de genre a été créé en 1867 par le protistologiste allemand Friedrich Johann Philipp Emil Ritter von Stein (1818-1885) à partir du préfixe latin [tintinnare] = tinter, sonner comme une clochette et du suffixe grec ancien [-opsis] = aspect, apparence, ressemblance. Ce nom signifie donc littéralement « qui a une forme de clochette ». Ce genre contient en effet de nombreuses espèces ayant l’allure d’une clochette, avec des bords plus ou moins évasés.
campanula : le nom spécifique campanula dérive du latin signifiant «
petite cloche », en référence directe à la morphologie caractéristique de la
lorica.
Numéro d'entrée WoRMS : 163913
| Termes scientifiques | Termes en français | Descriptif | |
|---|---|---|---|
| Embranchement | Ciliophora | Ciliés | Organismes unicellulaires eucaryotes (possédant un ou plusieurs noyaux) munis de flagelles, cils ou organes ciliés. Ils vivent en eau douce, saumâtre ou salée, modes de vie très variés. Certains sont photosynthétiques. |
| Sous-embranchement | Intramacronucleata | Intramacronucléate | |
| Classe | Oligotrichea | Oligotriches | |
| Sous-classe | Oligotrichia | ||
| Ordre | Choreotrichida | ||
| Sous-ordre | Tintinnina | Tintinnine | |
| Famille | Codonellidae | Codonellidés ou Codonellides | |
| Genre | Tintinnopsis | ||
| Espèce | campanula |
 Animaux unicellulaires
Animaux unicellulaires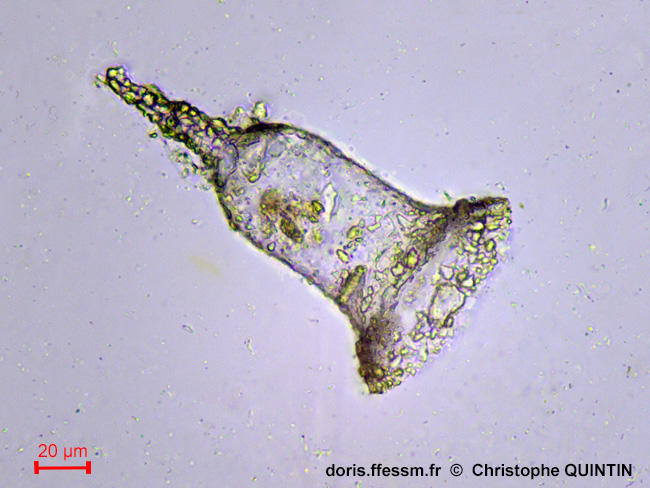
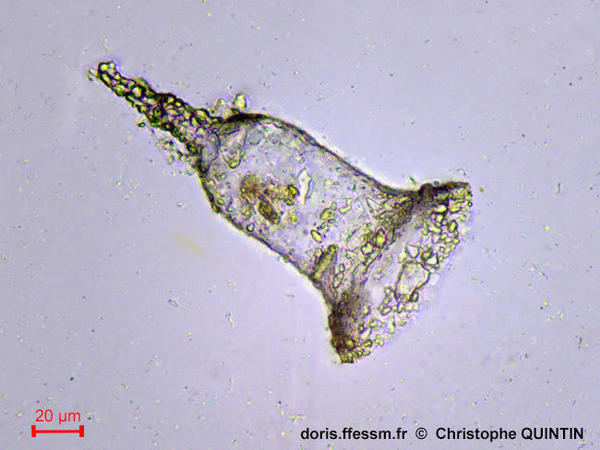
Vue au microscope d'une lorica
La lorica* de Tintinnopsis campanula présente une forme de cloche très facilement reconnaissable. Des grains de quartz ou d’autres particules solides sont collés de manière irrégulière sur la membrane.
Individu
capturé, au filet à plancton, dans le port de Binic (22).
Photographie
prise au microscope (objectif x40) composée par empilement de plusieurs photos
pour avoir une profondeur de champs couvrant la totalité du spécimen.
12/09/2025
 Animaux unicellulaires
Animaux unicellulaires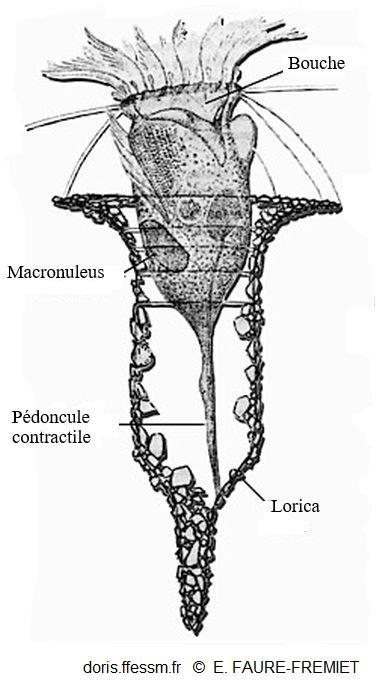
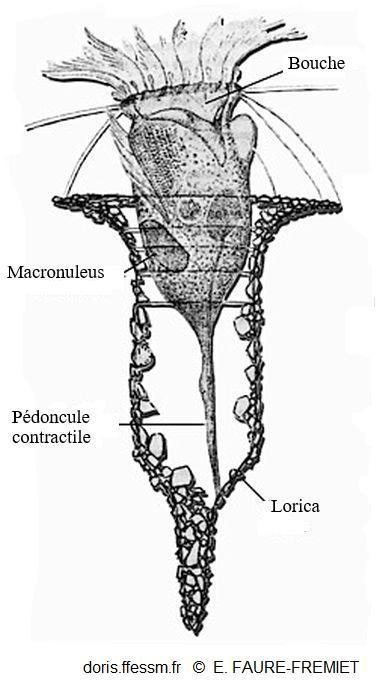
Vue en coupe de Tintinnopsis campanula
Ce dessin montre la morphologie de base des tintinnides.
La lorica* est recouverte de petites particules minérales, une extrémité est fermée et la lorica ne comporte pas d'épines ou de collerettes hyalines.
Dessin de Emmanuel Fauré-Fremiet in Contribution à la connaissance des Infusoires planktoniques
Reproduction de documents anciens
1924


Vue au microscope de deux loricas
La lorica* de Tintinnopsis campanula présente une forme de cloche très facilement reconnaissable.
Individus capturés, au filet à plancton, dans le port de Binic (22).
Photographie prise au microscope (objectif x40) composée par empilement de plusieurs photos pour avoir une profondeur de champs couvrant la totalité des spécimens..
16/09/2023


Vue au microscope de Tintinnopsis bütschlii souvent considéré comme une forme particulière de Tintinnopsis campanula.
Chez Tintinnopsis bütschlii la «queue» n’est pas présente du côté aboral de la lorica.
Individu capturé, au filet à plancton, dans le port de Binic (22).
Photographie prise au microscope (objectif x40).
16/09/2023
Rédacteur principal : Christophe QUINTIN
Vérificateur : Maurice HULLÉ
Responsable régional : Yves MÜLLER
Abou Zaid M., Hellal A., 2012, Tintinnids (Protozoa: Ciliata) from the coast of Hurghada Red Sea, Egypt, Egyptian Journal of Aquatic Research, 38, 249–268.
Bachy C., Gómez F., López-García P., Dolan J., Moreira D., 2012, Molecular Phylogeny of Tintinnid Ciliates (Tintinnida, Ciliophora), Protist, 63, 873–887.
Bakker C, Phaff W.J., 1976, Tintinnida from coastal waters of the S.W.-Netherlands I- The genus Tintinnopsis Stein, Hydrobiologia, 50,101–111.
Burkovsky I., Zamyshlyak Y., Poskryakova N., 1976, Revision of the fauna of Tintinnida (Ciliata) of the White Sea, Fisheries and Marine Service Translation Series, No. 3639, 20p.
Chovgan O., 2019, Review of tintinnid species (Ciliophora: Tintinnina) from the Barents Sea, Protistology 13 (3), 159–165.
Coats D., BachvaroffT., DelwicheC., 2012, Revision of the Family Duboscquellidae with Description of Euduboscquella crenulata n. gen., n. sp. (Dinoflagellata, Syndinea), an Intracellular Parasite of the Ciliate Favella panamensis Kofoid & Campbell, The Journal of eukaryotic microbiology, 59, 1-11.
Dolan J., 2010, Morphology and Ecology in Tintinnid Ciliates of the Marine Plankton: Correlates of Lorica Dimensions, Acta Protozoologica, 49, 235–244.
Dolan J., Montagnes D., Agatha S., Coats D., Stoecker D., 2013, The biology and ecology of Tintinnid ciliates, models for marine plankton, Wiley-Blackwell, 296 pp.
Durmus T., Balci M., Balkis N., 2011, Species of genus Tintinnopsis Stein, 1867 in Turkish coastal waters and new record of Tintinnopsis corniger Hada, 1964, Pakistan Journal of Zoology, 44(2), 383-388.
Ehrenberg C. G., 1840, Characteristik von 274 neuen Arten von Infusorien, Bericht über die zur Bekanntmachung geeigneten Verhandlungen der Königlich Preussischen Akademie der Wissenschaften zu Berlin, 197-219.
El-Damhougy K.A., El-Sayed A.A., Aboul Ezz S.M., Abu Husein M.S., 2017, Tintinnida (Ciliophora) as bio-indicator for certain pollutants at al-max area, Alexandria, Egypt, International Journal of Fisheries and Aquatic Studies, 5(3), 297-305.
Fauré-Fremiet E., 1924, Contribution à la connaissance des Infusoires Planktoniques, Bulletin Scientifique de la France et de la Belgique, supplément 6, 61-171.
Feng M., Zhang W., Wang W., Zhang G., Xiao T., Xu H., 2015, Can tintinnids be used for discriminating water quality status in marine ecosystems? Marine Pollution Bulletin, 101, 549-555.
Hofker J., I93I, Studien über Tintinnoidea, Archiv für Protistenkunde, 75, 315-402.
Jonsson P., 1989, Vertical distribution of planktonic ciliates - an experimental analysis of swimming behaviour, Marine Ecology Progress Series, 52, 39-53.
Kofoid C., Campbell A., 1929, A conspectus of the marine and freshwater ciliata belonging to the suborder Tintinnoinea, with descriptions of new species principally from the Agassiz Expedition to the Eastern Tropical Pacific 1904-1905, University of California Press.
Kufferath H., 1950, Recherches sur le plancton de la mer flamande (Mer du nord méridionale), I.- Quelques flagellés, protistes et « caetera », Institut Royal des Sciences Naturelles de Belgique, Bruxelles, XXVI, 29, 43p.
Li Z., Yi Z., Yang J., Gong J., Clamp J., Khaled A.S., Al-Rasheid K., Abdulaziz A., Alarifi S., Al-Khedhairy A., Song W., 2009, Phylogenetic investigation on five genera of tintinnid ciliates (Ciliophora, Choreotrichia), based on the small subunit ribosomal RNA gene sequences, Progress in Natural Science, 29, 1097-1101.
Meunier A., 1919, Microplankton de la Mer Flamande: 4 - Les Tintinnides et cœtera. Mémoires du Musée Royal d'Histoire Naturelle de Belgique = Verhandelingen van het Koninklijk Natuurhistorisch Museum van België, VIII(2), Hayez, imprimeur de l'Académie royale de Belgique: Bruxelles, 60p., 2 plates.
Monti-Birkenmeier M., Diociaiuti T., Fonda Umani S., 2019, Long-term changes in abundance and diversity of tintinnids in the Gulf of Trieste (Northern Adriatic Sea), Nature Conservation, 34, 373–395.
Nakamachi M., Iwasaki N., 1998, List of tintinnids (Protozoa: Ciliata) in Uranouchi Inlet, Kochi, Japan, Bulletin of marine sciences and fisheries, Kochi University, 18, 65-76.
Paulmier G., 1965, Le microplancton de la rivière d’Auray, Revue des travaux de l’Institut des Pêches Maritimes, 29 (2), 211-224.
Santoferrara L., Alder V., McManus G., 2017, Phylogeny, classification and diversity of Choreotrichia and Oligotrichia (Ciliophora, Spirotrichea), Molecular Phylogenetics and Evolution, 112, 12–22.
Snoeybos-West O. L. O., Salcedo T., McManus G. B., Katz L., 2002, Insights into the diversity of choreotrich and oligotrich ciliates (class Spirotrichea) based on genealogical analyses of multiple loci, International Journal of Systematic and Evolutionary Microbiology, 52, 1901–1913.
Taniguchi A., 1978, Reproduction
and life histories of tintinnid ciliates, Bulletin of Plankton Society of Japan, 25, 123-134.
Wang R., Song W., Bai Y., Warren A., Li L., Hu X., 2020, Morphological redescriptions and neotypification of two poorly known tintinnine ciliates (Alveolata, Ciliophora, Tintinnina), with a phylogenetic investigation based on SSU rRNA gene sequences, International Journal of Systematic And Evolutionary Microbiology, 70, 2515–2530.
Les textes et images sont sous licence et ne sont pas libres de droit.
Pour les ayants-droits, connectez-vous.
Pour toute demande d'utilisation (exemple d'un formateur Bio de la FFESSM...) contactez nous ici.