Minuscule fougère (pouvant atteindre 2 cm) flottante
Peut former un tapis dense à la surface de l’eau
Tige principale courte, allongée horizontalement et dichotome
Plante verte à rouge avec feuilles comme des écailles disposées en deux rangées alternées
Une racine filiforme pend sous chaque nœud de la tige
Symbiose avec des cyanobactéries
Azolle fausse fougère, azolla fausse
fougère, azolle rouge, fougère d'eau, azolla flottante, azolle fausse filicule,
azolla fausse filicule.
Red azolla, water fern, carolina fern, duck fern, duckweed fern, fairy fern, fairy moss, feathered water fern, mosquito fern, pacific mosquito fern, red water fern, water velvet (GB + Etats-Unis d'Amérique + Australie) ; Azolla maggiore (I) ; Rote Schwimmfarn, Grosser Algenfarn (D) ; Helecho de agua rojo, helecho de agua, heleechito del agua, helecho de pato (E) ; Rode vlotvaren, grote kroosvaren (NL) ; Andematbregne (Danois et Norvégien) ; Limaskasaniainen (Finnois) ; Go-prasad (Hindi et Marathi) ; šakotoji azolė (Lithuanien) ; Азолла (Russe) ; Mossbräken (Swiss – German-speaking Canton)
Azolla arbuscula Desv.
Azolla filiculoides var. filiculoides
Azolla japonica (Franch. & Sav.) Franch. & Sav. ex Nakai
Azolla magellanica Willd.
Azolla pinnata var. japonica Franch. & Sav.
Azolla squamosa Molina
Azolla caroliniana Willd. (synonyme pour certaines sources, taxon valide pour d'autres comme le GBIF).
Cosmopolite tropical et tempéré des eaux douces
Zones DORIS : ● Eau douce d'Europe, ○ [Guyane française]Cette espèce est présente en eau douce en Europe, en Guyane et à La Réunion et potentiellement partout dans l'ultramarin tropical et tempéré.
L'espèce serait originaire d'Amérique subtropicale et tempérée. Suite à son transport par l'Homme, elle est devenue plus ou moins cosmopolite en milieu tropical à tempéré. C'est l'espèce d'Azolla qui résiste le mieux au froid et qui remonte le plus haut en altitude et en latitude ; elle a été observée jusqu'à 5 000 m d'altitude dans les Andes sud-américaines ; en Europe, il y a des signalements en Ecosse et en Scandinavie. Elle a été introduite en Europe vers la fin des années 1870 ; en France, la première observation aurait été faite dans les Deux-Sèvres en 1880.
Dans les îles Britanniques (Middlesex), elle a été observée en 1883. Elle s'est rapidement naturalisée partout en Europe et y est localement envahissante. Dans les zones sous juridiction française, elle a été signalée en Guyane, où elle est native, et a été introduite à La Réunion ; elle pourrait être également présente dans tous les territoires tropicaux. Elle est absente, à ce jour, aux Antilles françaises.
Cette plante aquatique flottante vit en eau calme ou à courant lent : canaux, fossés, étangs, rizières, mares, bras morts (boires) de rivières. Elle préfère des eaux douces riches en nutriments (milieux eurythermes* mésotrophes* à eutrophes*) et des températures modérées à chaudes. Elle tolère mal l’eau salée et les eaux trop froides.
Cette minuscule fougère flottante mesure jusqu’à 2 cm de long. Les plantes sont imbriquées et forment un tapis dense à la surface de l’eau. L'azolle fausse-fougère est une plante pérenne délicate, finement découpée. Sa couleur varie au fil des saisons ; elle est verte (au printemps) et vire progressivement au rose, voire au rouge pourpre ou violacé-lie-de-vin (à l'automne). La couleur change aussi en fonction de l’exposition au soleil ou par grand froid ; des éclairements intenses produisent une couleur rouge. Le rhizome* est court et ramifié. La tige principale est très courte, allongée horizontalement ; elle se divise de façon dichotome* donnant à la plante un aspect en éventail. Les feuilles ressemblent à des écailles ; elles sont très serrées, imbriquées, disposées en deux rangées alternées le long de la tige ; elles sont minuscules (0,5 à 1,5 mm), triangulaires à ovales, à sommet obtus. Chaque feuille est bilobée avec un lobe* dorsal flottant, aérifère et des poils transparents hydrophobes retenant l’air et permettant la flottaison. Les lobes dorsaux ont des cavités abritant des cyanobactéries* symbiotiques*. Le lobe ventral est immergé, plus mince, chlorophyllien*. Une seule racine filiforme pend sous chaque nœud de la tige ; cette racine possède une coiffe à l’extrémité.
Au niveau mondial, le genre Azolla comporterait 5 à 7 espèces difficiles à distinguer les unes des autres ; une révision taxonomique du genre serait souhaitable pour clarifier les espèces et les synonymies ; il existerait des hybrides entre ces espèces (comme par exemple : A. cristata x A. filiculoides...).
- Azolla filiculoides est la plus souvent citée et sans doute la plus commune.
- Azolla cristata est commune en Amérique, difficile à distinguer de A. ficuloides sans microscope.
Les autres espèces reconnues actuellement sont :
- Azolla caroliniana est considérée comme distincte par de nombreuses bases en lignes, comme le GBIF ; indigène des Amériques, quelques introductions citées en Thaïlande et Vietnam. En fait, les phylogénies* moléculaires distinguent bien caroliniana de filiculoides,
- Azolla mexicana (Amériques et Europe),
- Azolla nilotica (Afrique),
- Azolla pinnata (Afrique, Asie du sud et Australie y compris la Nouvelle-Calédonie),
- Azolla rubra (Australie et Nouvelle-Zélande).
Dans la même famille des Salviniacées (aussi appelée parfois Azollacées), il n'existe qu'un autre genre principal, le genre Salvinia. Salvinia natans est une autre fougère aquatique flottante, mais avec des feuilles plus grandes et différentes des feuilles en écaille de A. ficuloides.
La confusion est éventuellement possible avec d'autres mini plantes "à fleurs" qui flottent également à la surface de l'eau. Citons les espèces suivantes dans la famille des lentilles d’eau.
- La petite lentille d'eau Lemna minor, autochtone*, lames de 1,5 à 6 mm de diamètre, planes, avec une seule racine, la plus commune.
- La lentille d'eau minuscule Lemna minuta, introduite en Europe (importée d'Amérique : 1965 en France). Les lames sont petites (0,8 à 4 mm) avec des bords minces et translucides.
- La lentille d'eau bossue Lemna gibba, autochtone 2 à 5 mm fortement renflée à la face inférieure.
- La lentille d'eau rouge Lemna turionifera, introduite en Europe (importée d'Amérique : 1983 en Allemagne). Elle descend en profondeur à l'automne et passe l'hiver sous forme de turions* qui remontent à la surface à partir de mars. Seule la base des racines et les turions ont cette couleur rouge due à la présence d'anthocyanine, un pigment végétal.
- La lentille d'eau à racines nombreuses Spirodela polyrhiza, espèce autochtone de 5 à 10 mm qui est ronde, épaisse, verte ou un peu rouge et possède 5 à 15 racines ; elle est faite de plusieurs (3 ou 4) disques assemblés en feuille de trèfle formant un ensemble grand comme un ongle.
- La wolffie sans racines Wolffia arrhiza, plante autochtone très petite (de 0,5 à 5 mm pour les plus grandes), verte, subsphérique et sans racine ; elle est assez rare.
Comme toutes les plantes chlorophylliennes, Azolla filiculoides est autotrophe* : elle réalise la photosynthèse*.
Elle vit en symbiose* avec une cyanobactérie fixatrice d’azote, Trichormus azollae (ex Anabaena azollae) qui lui fournit l’azote nécessaire à sa croissance et lui permet ainsi de prospérer dans des milieux pauvres en nutriments azotés. Cette symbiose "algue bleue-fougère" est rare dans le monde vivant. Elle rappelle un peu les symbioses "algue bleue-champignon" ou "algue verte-champignon" des lichens ou des associations "champignons-algues" de quelques macro algues marines.
Cette plante hétérosporée est souvent stérile ; elle produit cependant parfois des mégaspores et des microspores contenues dans des petits organes ovoïdes, les sporocarpes*, fixés sous les feuilles ou aux aisselles foliaires. Les mégasporocarpes contiennent une seule mégaspore entourée de poils crochus (nommés glochidies* en botanique) favorisant l’attachement et la dispersion. Les microsporocarpes contiennent de nombreuses microspores.
En ce qui concerne la multiplication végétative, la plante se fragmente naturellement et chaque fragment peut produire une nouvelle colonie. C’est sa principale stratégie de multiplication végétative. La croissance est très rapide : la biomasse peut doubler en 2 à 5 jours dans de bonnes conditions.
La reproduction sexuée par production de spores* résistantes à la dessiccation est apparemment très peu fréquente en France. Elle a lieu au printemps ou de juillet à octobre ou toute l'année (selon les sources) en produisant des sortes de ''fruits'', les sporocarpes* qui contiennent les spores. Les spores sont souvent peu viables en climat tempéré.
L'azolle fausse-fougère sert d'abri pour la faune aquatique : vers, gastéropodes, insectes et leurs larves*, crustacés, etc. Les tapis denses qu'elle forme réduit ou empêche le développement d'algues et de plantes aquatiques submergées.
En surface, elle peut cohabiter avec des petites lentilles d'eau qui lui ressemblent comme Lemna minuta, L. minor ou L. minuscula ou encore comme Wolffia arrhiza qui flotte aussi à la surface de l'eau. Les tapis denses empêcheraient les larves* de moustique d'émerger de l'eau lors de la métamorphose*.
Le charançon Stenopelmus rufinasus introduit (venu d'Amérique) est un prédateur très spécifique d'A. ficuloides. Il est utilisé pour en contrôler les populations, en particulier en Afrique du Sud. Des opérations de lutte biologique à l'aide de cet insecte ont eu lieu en Europe (en Grande-Bretagne, Belgique et Pays-Bas). De telles opérations sont seulement envisagées en France actuellement.
Comme les lentilles d'eau et certains crustacés des marécages, l'azolle fausse-fougère peut être transportée sur les pattes des oiseaux lors de leurs déplacements locaux ou de leurs migrations saisonnières. Ceci explique la dispersion souvent rapide de ces espèces d'un plan d'eau à un autre ou d'une région à l'autre. La dispersion naturelle peut intervenir via la faune mobile mais elle est surtout le fait des activités anthropiques : transport des plantes d'ornement aquatiques, aquariophilie, déplacements liés à la pêche en eau douce, activités nautiques, ballast des navires.
Cette plante est utilisée comme engrais vert dans les rizières d’Asie (riziculture). Elle possède une très forte capacité à accumuler les métaux lourds et les polluants, ce qui lui permet d’être utilisée en phytoremédiation*. Elle peut devenir envahissante en formant des nappes denses qui étouffent les milieux aquatiques.
Cette minuscule fougère est assez particulière dans la mesure où elle est très fugace et imprévisible dans son comportement. Elle apparaît ici ou là, puis disparaît l'année suivante et peut réapparaître quelques kilomètres plus loin. Elle peut proliférer certaines années et devient alors envahissante. Son contrôle, voire son éradication, peut se faire par différents moyens ; le moissonnage des tapis est possible en cas de nécessité.
Cette plante est utilisée en aquariophilie ou pour la production de biomasse en raison de sa croissance rapide.
La fausse-fougère aquatique n'est pas toxique sauf cas particuliers (plantes en pourriture) ; c'est une nourriture possible pour le bétail, les poissons et les oiseaux d'eau (cygnes, oies, canards...).
Les fossiles montrent que la relation entre la plante et la cyanobactérie a été établie à l'époque des dinosaures (au Crétacé) et que plante et cyanobactérie ont coévolué pendant des millions d’années.
En France, l'espèce est soumise à règlementation agricole : arrêté du 13 juillet 2010 relatif aux règles de bonnes conditions agricoles et environnementales (BCAE). Azolla filiculoides est aussi inscrite sur la liste de consensus du Code de conduite professionnel relatif aux plantes exotiques envahissantes.
Cette plante invasive est interdite ou réglementée dans certains pays, notamment en Australie.
Azolle : dérivé du nom de genre en latin Azolla.
Fausse fougère : bien qu’elle soit taxonomiquement une fougère, elle ne possède pas tous les traits typiques des fougères terrestres.
Azolla, nom dont l’étymologie est incertaine. Lors de la description de cette plante du Chili ou d'Argentine, le naturaliste français Jean-Baptiste Pierre Antoine de Monet, chevalier de Lamarck (1744-1829), n'a pas donné l'origine de ce nom. Il a juste mentionné : "Cette plante a été rapportée de Magellan par M. de Commerson". Philibert Commerson (1727-1773) est un naturaliste français qui a beaucoup voyagé.
filiculoides : du latin [filix] = fougère et du suffixe [-oides] = qui ressemble a, signifie « qui ressemble à une fougère".
Numéro d'entrée WoRMS : 1633949
| Termes scientifiques | Termes en français | Descriptif | |
|---|---|---|---|
| Embranchement | Tracheophyta | Trachéophytes | |
| Sous-embranchement | Polypodiophytina | ||
| Classe | Polypodiopsida | ||
| Sous-classe | Polypodiidae | Polypodidés | |
| Ordre | Salviniales | Salviniales | |
| Famille | Salviniaceae | Salviniacées | |
| Genre | Azolla | ||
| Espèce | filiculoides |


Vue générale des plantes avec feuilles écailleuses
L'azolle fausse-fougère flotte à la
surface de l'eau. Noter au centre la couleur rouge de la plante et la couleur
verte périphérique des parties les plus jeunes.
Guînes (Pas-de-Calais, 62) devant l'écomusée
16/04/2025


Habitat
Vue générale montrant un fossé
complètement recouvert d'un tapis continu d'individus très serrés de l'azolle
fausse-fougère.
Guînes (Pas-de-Calais, 62) devant l'écomusée
16/04/2025


Lentille d'eau et azolle fausse-fougère
La lentille d'eau (Lemna minor) au centre de l'image donne une idée de la petite taille de la fougère.
Guînes (Pas-de-Calais, 62) devant l'écomusée
16/04/2025


La partie immergée
Une vue latérale ex-situ montre les racines submergées ; elles peuvent atteindre 2 cm.
Guînes (Pas-de-Calais, 62) devant l'écomusée
16/04/2025


Détail des racines
Une vue à la loupe de jeunes racines
permet de voir la coiffe au bout de la racine
Guînes (Pas-de-Calais, 62) devant l'écomusée
16/04/2025
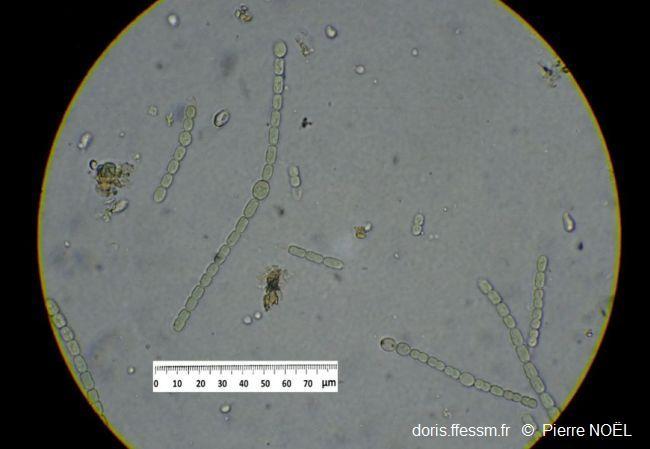
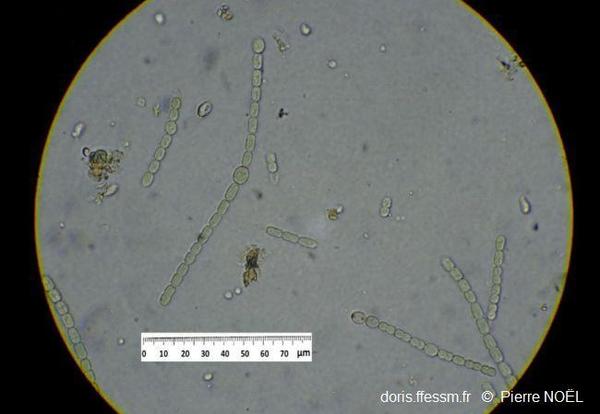
L'algue bleue symbiotique
Une vue au microscope montre la cyanobactérie fixatrice d’azote, Trichormus azollae. Ses filaments mesurent jusqu'à 300 μm de long. Les hétérocytes (cellules ovoïdes) mesurent environ 7 x 10 μm.
Au microscope, Guînes (Pas-de-Calais, 62) devant l'écomusée
16/04/2025

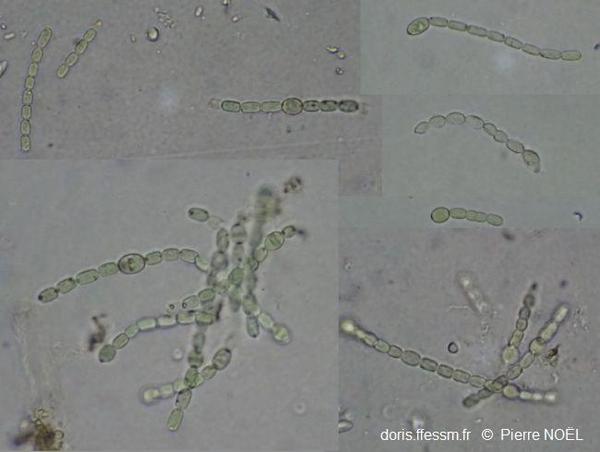
Détails des filaments de l'algue bleue symbiotique
Les hétérocytes (cellules ovoïdes) peuvent
apparaître terminaux suite à la rupture des filaments lors de la dissection des
feuilles de la fougère. Ils sont normalement dans le filament.
Guînes (Pas-de-Calais, 62) devant l'écomusée
16/04/2025
Rédacteur principal : Pierre NOËL
Correcteur : Jean-Yves DUBUISSON
Responsable régional : Yves MÜLLER
Abbayes H. des, Chadefaud M., Ferré Y. de, Feldmann J., Gaussen H., Grassé P.-P., Leredde M. C., Ozenda P., Prévot A. R., 1963, Botanique. Anatomie - cycles évolutifs systématique. Précis de sciences biologiques publiés sous la direction du Pr Pierre-P. Grassé, Masson et Cie, Editeurs, Paris, 1-1040.
Bange A. J., Bange C., 1955, Sur la distribution des Azolla en France et dans les pays voisins, Publications de la Société Linnéenne de Lyon, 24(5), 129-133.
Barbe J., 1984, Les végétaux aquatiques. Données biologiques et écologiques. Clés de détermination des macrophytes de France, Bulletin Français de Pisciculture, 1-42.
Bonnier G., de Layens G., 1948, Flore complète portative de la France, de la Suisse et de la Belgique, Librairie générale de l’enseignement, Paris, 427 pp.
Boudet L., Bange A. J., 1949, Sur les Azolla de la région lyonnaise, Publications de la Société Linnéenne de Lyon, 18(10), 218-219.
Branquart E., Fried G., 2016, Les espèces envahissantes d'ici et d'ailleurs : Synthèse sur les espèces envahissantes et présentation de 32 espèces, préface de Daniel Simberloff, Editions du Gerfaut, 192 pp.
CBNMed, 2021, Azolla filiculoides [en ligne], INVMED-Flore, plateforme sur les invasions biologiques végétales, Conservatoire botanique national méditerranéen et Conservatoire botanique national de Corse, Disponible sur :https://invmed.fr/src/listes/evee-fiche.php?cd_ref...
Coste H., 1899-1906, Flore descriptive et illustrée de la France, de la Corse et des contrées limitrophes, Albert Blanchard, Paris, (3 vol.), 1852 pp.
Denis M., 1925, Contribution à la flore algologique de l'Auvergne, Bulletin de la Société Botanique de France, 72(4), 876-887.
Desvaux A. N., 1827, Prodrome de la Famille des Fougères, Mémoires de la Société linnéenne de Paris, vi, 171-337.
Dutartre A., Haury J., Planty-Tabacchi A. M., 1997, Introductions de macrophytes aquatiques et riverains dans les hydrosystèmes français métropolitains: essai de bilan, Bulletin Français de la Pêche et de la Pisciculture, 344/345, 407-426.
Felzines J.C., Loiseau J.-E., 1991, Une association à Lemna minuscula et Azolla filiculoides dans les vallées de la Loire Moyenne et du Bas-Allier, Le Monde des plantes, 7(441), 6-9.
Haury J., Thiébaut G., Coudreuse J., Muller S., 2007, Les lichens, bryophytes, ptéridophytes et phanérogames aquatiques, Sciences Eaux & Territoires (Spécial Ingénieries-EAT-25), 23-36.
Jaeger P., 1952, Note provisoire sur le comportement de l'Azolla filiculoides Lmk. dans le système du confluent de l'Ill (région de Strasbourg), Le Monde des plantes, 7(283-284), 61-62.
Lamarck, J.-B.P.A. de M. de., 1783, Encyclopédie méthodique. Botanique. Tome premier, A Paris, chez Panckoucke, libraire, Hôtel de Thou, rue des Poitevins, 752 pp.
Lambinon J., Delvosalle L., Duvigneaud J. , 2004, Nouvelle Flore de la Belgique, du Grand-Duché de Luxembourg, du Nord de la France et des Régions voisines (Ptéridophytes et Spermatophytes). Cinquième édition, Meise, Ed. du Patrimoine du Jardin botanique national de Belgique, 1167 pp.
Muller S., 2006, Prolifération spectaculaire d’Azolla filiculoides (Azollaceae, Pteridophyta) dans le canal de Jouy près de Metz (Lorraine, France) à l’automne 2005, Bulletin de la Société des Naturalistes Luxembourgeois, 107, 31.
Pieret, N., Delbart, E., & Mahy, G., 2009, Fiches descriptives des principales espèces de plantes invasives: Azolla filiculoides, Cellule d’appui à la gestion des plantes invasives - Proposition de méthodes de gestion préventives et actives de la problématique des plantes invasives aux abords des cours d’eau non navigables en Région wallonne, 1-3.
Préfecture de la région des Pays de la Loire, 2009, Espèces exotiques et envahissantes des cours d'eau des pays de la Loire, synthèse des données invertébrés, macrophytes et diatomées 2007-2008, Aquascop, 6936, 1-41.
Rioux J.-A., Quézel P., 1950, Fructification synchrone d'Azolla filiculoides dans le Bas-Languedoc, Le Monde des plantes, 7(269), 42.
Roze E., 1883, Contribution à l'étude de la fécondation chez les Azolla, Bulletin de la Société Botanique de France, 2, Tome 30 - Fascicule 1, 198- 206.
Roze E., 1888, Recherches biologiques sur l'Azolla filiculoides Lamk. Bulletin de la Société Botanique de France, 2, Tome 35 - Fascicule 1, 427-428.
Vanderhoeven S., Branquart E., Mahy G., Grégoire J.C., 2006, L'érosion de la biodiversité ; les espèces exotiques envahissantes, Dossier scientifique réalisé dans le cadre de l’élaboration du Rapport analytique 2006 sur l’État de l’Environnement wallon. FUSAGx, CRNFBGx et ULB, 42 pp.
La page sur Azolla filiculoides dans l'Inventaire National du Patrimoine Naturel : INPN
Les textes et images sont sous licence et ne sont pas libres de droit.
Pour les ayants-droits, connectez-vous.
Pour toute demande d'utilisation (exemple d'un formateur Bio de la FFESSM...) contactez nous ici.