Texture douce, soyeuse, gélatineuse
Fixé au substrat par un disque réduit
Stipe cylindrique très court
Deux à trois grandes lames souples, lancéolées
Proliférations lancéolées sur les marges
Couleur rouge foncé à brunâtre
Longueur du thalle 80 à 150 cm
Largeur de la fronde 5 à 15 cm
Grateloupe chinoise
Devil's tongue weed, Asian red seaweed (GB, Slijmerige drakentong (NL)
Halymenia sinensis C.K.Tseng & C.F.Chang, 1984
Atlantique, Asie du Sud-Est, Australie, Nouvelle-Zélande
Zones DORIS : ● Europe (côtes françaises), ○ [Atlantique Nord-Est, Manche et mer du Nord françaises], ● Caraïbes, ○ [Méditerranée française]Originaire de l’Asie du Sud-Est, elle s’est répandue sur toutes les côtes européennes de la Suède au Portugal en Atlantique Nord-Est ainsi qu’en Méditerranée. Sa présence a été remarquée également en Atlantique Nord-Ouest du Canada au nord jusqu’aux États-Unis au sud ainsi qu’en Martinique. On l’observe aussi dans le Pacifique : en Australie, en Nouvelle-Zélande et au Chili.
Cette espèce vit dans des biotopes* photophiles* superficiels du haut de l’estran* jusqu’à 7 m de profondeur environ. Elle a la capacité à occuper aussi bien des habitats exposés ou des lagunes littorales.
En outre elle colonise des substrats* naturels (roches, pierres, coquillages…) ou artificiels (épaves, pontons portuaires…).
Elle est tolérante aux écarts de température, de salinité, d’intensité lumineuse et de conditions trophiques*.
Le thalle* de l’algue rouge Grateloupia turuturu possède une texture douce, soyeuse, gélatineuse et mucilagineuse*. Il est fixé au substrat* par un disque réduit de 1 à 2 mm de diamètre d’où part un stipe* cylindrique très court de 2 à 5 mm de longueur.
La fronde* se divise en deux à trois grandes lames épaisses mais souples, lancéolées*, aux contours ondulés. Elles sont ornées sur les marges de proliférations en forme de fer de lance irrégulièrement disposées.
La couleur de cette rhodophycée est rouge foncé à brunâtre.
La longueur du thalle peut atteindre 80 à 150 cm voire exceptionnellement 300 cm dans des milieux favorisés (ex. île Callot dans la baie de Morlaix dans le Finistère). La largeur de la fronde oscille entre 5 et 15 cm pour une épaisseur de 225 à 580 µm.
En coupe, l’algue présente un cortex* de petites cellules pigmentées et une médulla* filamenteuse lâche.
Cryptonemia hibernica Guiry & L.M.Irvine, 1974 : les frondes* ont tendance à avoir une forme distinctement ovale et les proliférations sont moins lancéolées.
Dilsea carnosa (Schmidel) Kuntze, 1898 : les lames sont nettement ovales, cartilagineuses et nettement coriaces. Les marges sont franches sans proliférations lancéolées.
Itonoa marginifera (J.Agardh) Masuda & Guiry, 1995 : les frondes se fractionnent irrégulièrement en de nombreuses lames qui se terminent par des divisions dichotomiques*. A chaque division la lame se rétrécit puis s’élargit créant des espaces en forme de trous de serrure entre les divisions. Les marges des lames sont exemptes de proliférations.
Palmaria palmata (Linnaeus) F.Weber & D.Mohr, 1805 : le thalle* de cette palmariale est nettement touffu et plus rigide, ses extrémités sont nettement bifides*. Sa couleur est plus pourpre et sa taille plus petite (40 cm de hauteur environ).
Schizymenia dubyi (Chauvin ex Duby) J. Agardh 1851 : le thalle très similaire se distingue aisément par la présence de nombreuses cellules sécrétrices réfringentes dans le cortex*.
Stenogramma interruptum (C.Agardh) Montagne, 1846 : on note la présence sur les lames principales d’une nervure centrale discontinue. La longueur du thalle (7 cm) et la largeur des lames (1 cm) sont nettement inférieures. Les lames se divisent régulièrement de manière dichotomique.
Cet organisme pluricellulaire autotrophe* et photosynthétique* tire son énergie de la lumière solaire, de l'absorption d'eau, de dioxyde de carbone, des différents pigments qu’elle contient dont le pigment rouge (phycoérythrine*), la chlorophylle* (vert) et les caroténoïdes* (jaune/brun) ainsi que des nutriments dissous dans l'eau (azote, phosphore). Elle fabrique ainsi la matière organique nécessaire à son développement.
Cette espèce se reproduit de manière sexuée. Elle est annuelle et ne se développe que l’été. Le cycle est trigénétique isomorphe*, c'est-à-dire que tétrasporophytes* et gamétophytes* sont morphologiquement identiques. Le gamétophyte produit à la fois des organes mâles et des organes femelles (thalle monoïque*). Après fécondation, les organes femelles développent des cystocarpes* enfouis dans le thalle et abritant le carposporophyte*. Les carpospores donnent naissance aux tétrasporophytes. Les tétrasporocystes, à division cruciée*, se différencient dans le cortex*. Une fois émises, les tétraspores redonnent des gamétophytes.
Dans son aire de répartition d’origine, la grateloupe turuturu a une taille moyenne de l’ordre d’une vingtaine de centimètres et ne prolifère pas autant, phénomène qui s’explique certainement par la présence de nombreuses espèces d’algues en compétition dans la même zone infralittorale. Le succès de son adaptation sur nos côtes semble dû à une croissance très rapide, un pouvoir de reproduction élevé, une grande aptitude à se fixer sur n'importe quel support solide, une faculté d'adaptation importante et de fortes capacités physiologiques.
Cependant bien que considérée comme une ENI (espèce non indigène) elle n’est pas tenue pour être invasive. Elle ne paraît pas avoir causé d’impacts écologiques notoires et aucune élimination d’espèces concurrentes n’a encore été observée (Plouguerné, 2006).
La dispersion de Grateloupia turuturu reste néanmoins préoccupante et la question de sa valorisation est au cœur d’études dont les avancées dans certains domaines semblent significatives (voir chapitre informations complémentaires).
Grateloupia turuturu est une espèce asiatique introduite accidentellement dans les années 1970 en Europe puis dans d’autres pays du Monde avec du naissain* d’huîtres japonaises. En France, sa présence a été identifiée en 1982 dans l'étang de Thau, puis en Bretagne, d’abord en 1989 dans le Morbihan puis en 1992 dans le Finistère. Son extension vers de nouvelles stations a été observée.
Des extraits de l’algue rouge Grateloupia turuturu ont été utilisés en tant que principe actif dans des produits cosmétiques, et notamment en tant qu'agent de ralentissement du vieillissement.
Cette macroalgue rouge, riche en protéines, est comestible ; elle est consommée usuellement comme légume de mer au Japon.
Sur les côtes bretonnes, où elle est disponible en quantités importantes, ses composés bioactifs et notamment sa richesse en fibres alimentaires offrent un gisement potentiel d’intérêt pour la nutrition humaine en tant qu’aliments fonctionnels et compléments alimentaires.
En Atlantique et en Méditerranée, elle fut longtemps signalée sous le nom erroné de Grateloupia doryphera (Montagne) M. Howe, 1914.
Grateloupe : en hommage à Jean-Pierre Sylvestre Grateloup (1782-1861), médecin, naturaliste et botaniste français.
turuturu : conservation de son nom latin.
Grateloupia : dédié à J.-P. S. Grateloup, botaniste français, spécialiste reconnu de cryptogamie*.
turuturu : onomatopée japonaise dont le sens fait allusion à quelque chose de lisse, glissant, poli. En rapport avec la texture douce et soyeuse de la fronde.
Numéro d'entrée WoRMS : 295880
| Termes scientifiques | Termes en français | Descriptif | |
|---|---|---|---|
| Embranchement | Rhodobionta / Rhodophyta | Rhodobiontes | Algues rouges, pour la plupart marines. |
| Sous-embranchement | Eurhodophytina | Eurhodophytinés | |
| Classe | Florideophyceae | Floridéophycées | Thalle élaboré formé de fins filaments branchés ou en lames. |
| Sous-classe | Rhodymeniophycidae | Rhodyméniophycidées | |
| Ordre | Halymeniales | Halyméniales | |
| Famille | Halymeniaceae | Halyméniacées | |
| Genre | Grateloupia | ||
| Espèce | turuturu |
 Algues rouges (Rhodophycées)
Algues rouges (Rhodophycées) Algues rouges (Rhodophycées)
Algues rouges (Rhodophycées)

Lames
Les lames sont ornées sur les marges de proliférations en forme de fer de lance irrégulièrement disposées.
Dreischor, Zélande, Pays-Bas, 2 m
21/06/2023


Plusieurs lames divisées
Cette algue rhodophyte possède une ou plusieurs lames, simples ou divisées.
Pornic (44), estran
27/08/2010


Rouge foncé
La couleur des lames est rouge foncé à brunâtre.
Ile Tatihou, Saint-Vaast-la-Hougue (50), médiolittoral inférieur
02/11/2013


Couleur inhabituelle
La couleur habituelle de Grateloupia turuturu est rouge foncé à brunâtre. La couleur vert pâle sur ce cliché est fréquente en Zélande.
Zélande, Pays-Bas, 3 m
15/07/2018


Cuvettes du médiolittoral
Cette espèce photophile vit à faible profondeur essentiellement dans les cuvettes du médiolittoral.
Sud du fort de l'Ilet, Ile Tatihou (50), estran
09/10/2021


Contours ondulés
La grateloupe turuturu forme de grandes lames souples, lancéolées, aux contours ondulés.
San Hougue, île Tatihou, Saint-Vaast-la-Hougue (50), médiolittoral inférieur
02/11/2013
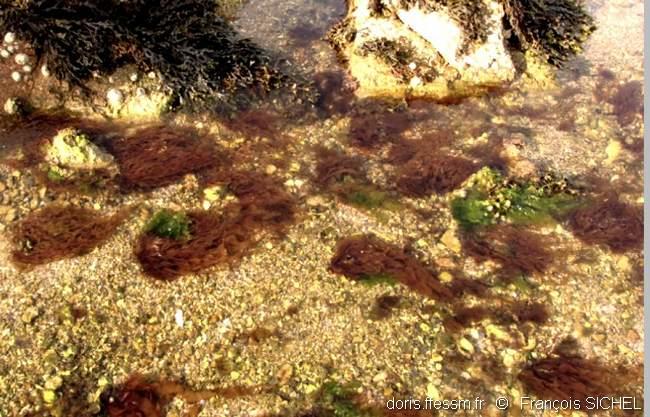

Biotope de l’estran
Cette espèce vit toute l’année dans des biotopes photophiles de l’estran, ici sur un fond de cailloutis.
Côte sud-est, Ile Tatihou (50), estran
23/09/2007


Fronde assez large
La largeur de la fronde oscille entre 5 et 15 cm pour une épaisseur de 250 à 580 µm.
San Hougue, île Tatihou, Saint-Vaast-la-Hougue (50), médiolittoral inférieur
02/11/2013


Biotope
Dans son aire de répartition d’origine, la grateloupe turuturu a une taille moyenne de l’ordre d’une vingtaine de centimètres et ne prolifère pas autant, phénomène qui s’explique certainement par d’excellentes conditions environnementales avec, comme sur ce cliché, la présence de nombreuses espèces d’algues en compétition dans la même zone infralittorale. Ici des Codium fragile.
Gemaal van Dreischor, Zélande, Pays-Bas, 2 m
27/08/2024


Reproduction ancienne
Deux thalles gamétophytes femelles récoltés à Muroran sur l’île japonaise d’Hokkaidō.
Planche 46 dans "Planche 46 dans "Notes on some Japanese algae IX" par Y. Yamada
Reproduction de documents anciens
1941
Rédacteur principal : Philippe LE GRANCHÉ
Correcteur : Marc VERLAQUE
Responsable régional : Philippe LE GRANCHÉ
Araújo de Azevedo C.A., Cassano V., Horta Júnior P.A., Batista M.B., Cabral de Oliveira M., 2015, Detecting the non-native Grateloupia turuturu (Halymeniales, Rhodophyta) in southern Brazil, Phycologia, 54, 5, 451-454.
Baffreau A., Pezy J.-Ph., Rusig A.-M., Mussio I., Dauvin J.-C., 2018,
Les espèces marines animales et végétales introduites en Normandie, Université
de Caen, Agence de l'eau Seine-Normandie (AESN), 348p.
Barnathan G., 2015, Valorisation d’espèces marines invasives : la grateloupe (algue rouge), la crépidule (gastéropode), Institut Océanographique de Monaco, 6p.
Denis C., 2009, Caractérisation biochimique de l'algue Grateloupia
turuturu, évaluation de ses potentialités de valorisation via un procédé de
digestion enzymatique et la purification partielle d'un pigment d'intérêt
(R-phycoétythrine), Thèse : biologie des organismes, École
doctorale Végétal-Environnement-Nutrition-Agro-Alimentaire-Mer (Angers), 306p.
García Bueno N., 2015, Valorisation de la macroalgue proliférante Grateloupia turuturu dans l’élevage de l’ormeau européen Haliotis tuberculata, Thèse de Doctorat, Ecole Doctorale Végétal, Environnement, Nutrition Agroalimentaire, Mer (VENAM), Faculté des Sciences et des Techniques, Université de Nantes, 264p.
Gavio B., Fredericq S., 2002, Grateloupia turuturu (Halymeniaceae, Rhodophyta) is the correct name of the non-native species in the Atlantic known as Grateloupia doryphora, European Journal of Phycology, U.K., 37, 349-360.
Katsanevakis S. et al., 2014, New Mediterranean Biodiversity Records (October, 2014), Mediterranean Marine Science, 15, 3, 675-695.
Munier M., 2013, Etude du polymorphisme pigmentaire de l'algue rouge Grateloupia turuturu au travers de la purification et la caractérisation de la R-Phycoérythrine en vue d'une valorisation industrielle, Thèse de doctorat : Biologie des organismes, Biochimie marine, Université de Nantes, 229p.
(Ouvrage collectif), 2022, Guide d’identification des espèces non-indigènes marines et des espèces en extension de répartition, Réseau Alien Mer Normandie, FFESSM Normandie, 12p.
Plouguerné E., 2006, Étude écologique et chimique de deux algues introduites sur les côtes bretonnes, Grateloupia turuturu Yamada et Sargassum muticum (Yendo) Fensholt : nouvelles ressources biologiques de composés à activité antifouling, Thèse de Doctorat de l’Université de Bretagne Occidentale (UBO), Mention : Chimie marine, 251p.
Stiger V., Thouzeau G., 2015, Marine Species Introduced on the French Channel-Atlantic Coasts: A Review of Main Biological Invasions and Impacts, Open Journal of Ecology, 5, 05, 227-257.
Stiger-Pouvreau V., Pagny J., 2008, La grateloupe (Grateloupia turuturu), Espèces invasives, Observatoire de la biodiversité et du patrimoine naturel en Bretagne, 2p.
Stiger-Pouvreau V., Le Lann K., Plouguerné E., Connan S., Deslandes E., 2015, Distribution et expansion de l’algue rouge introduite Grateloupia turuturu sur le littoral des côtes Ouest de la France – potentiel de valorisation ?, Rencontres Physiologiques de France, 1p.
Verlaque M., Brannock P.M., Komatsu T., Villalard-Bohnsack M., Marston M., 2005, The genus Grateloupia C. Agardh (Halymeniaceae, Rhodophyta) in the Thau Lagoon (France, Mediterranean): a case study of marine plurispecific introductions, Phycologia, 44, 477–496.
Yamada Y., 1941, Notes on some Japanese algae IX, Scientific Papers of the Institute of Algological Research, Faculty of Science, Hokkaido Imperial University, 2, 195-215, 15 figs, pls 40-48.
La page de Grateloupia turuturu sur le site de référence de DORIS pour les algues : AlgaeBase
La page de Grateloupia turuturu sur le site de référence de DORIS pour les algues : WoRMS
Les textes et images sont sous licence et ne sont pas libres de droit.
Pour les ayants-droits, connectez-vous.
Pour toute demande d'utilisation (exemple d'un formateur Bio de la FFESSM...) contactez nous ici.